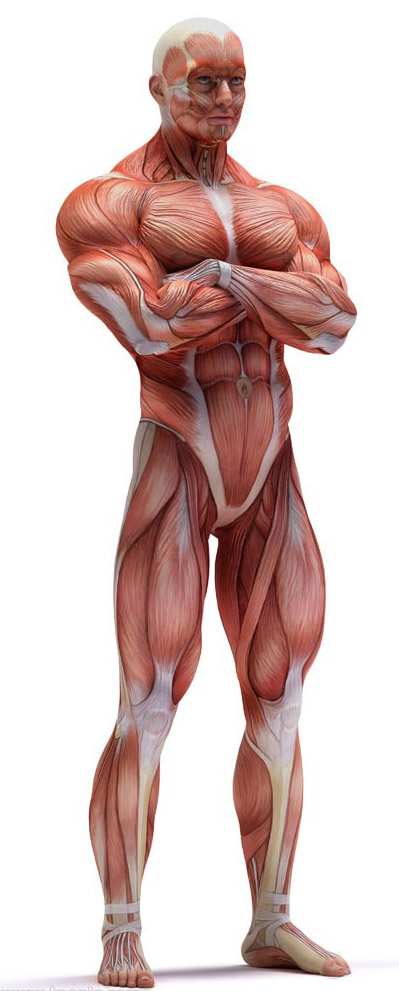
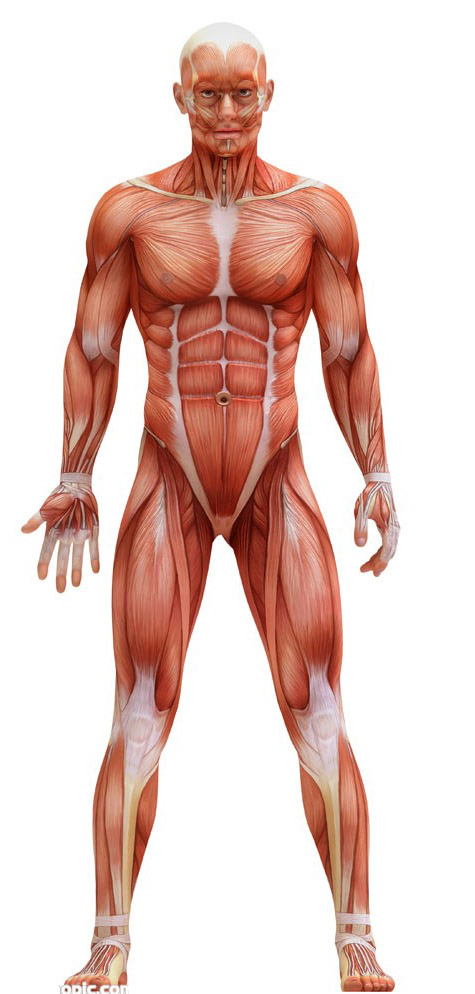
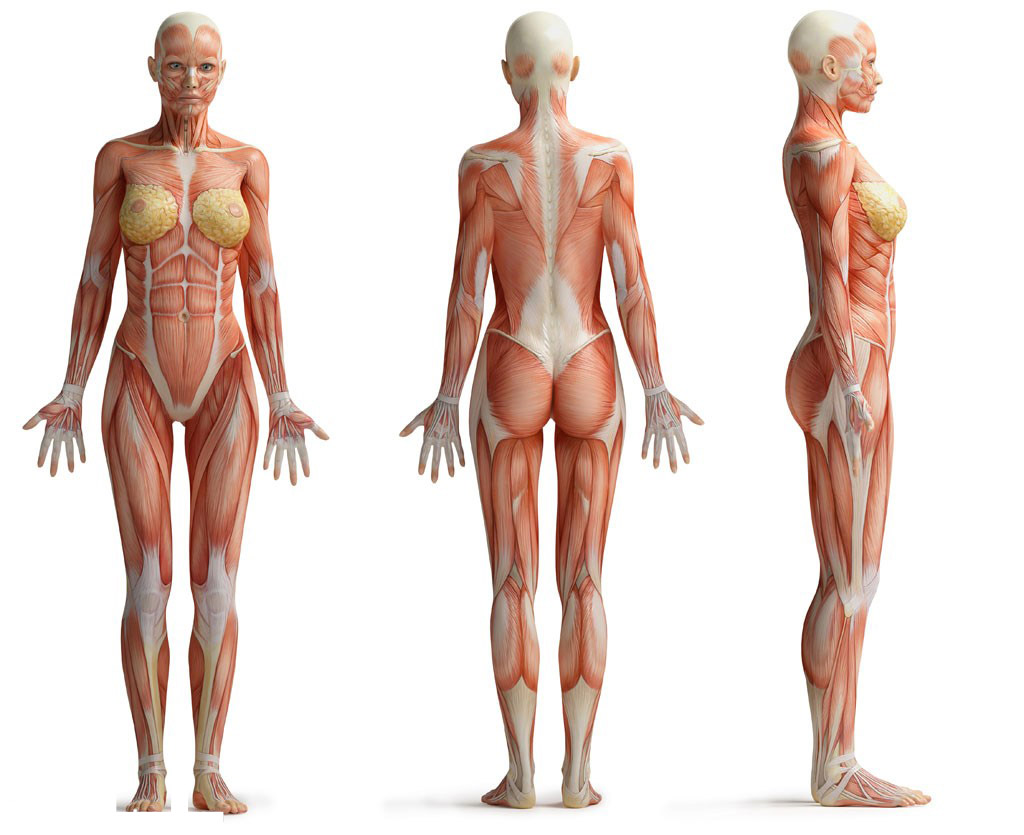
高血压是脑卒中的主要危险因素,在我国高血压的主要转归为脑卒中,其发病率是心肌梗塞的5倍。脑卒中的发生与高血压程度及持续的时间有着密切的关系。血压的增高不论是收缩压(SBP)还是舒张压(DBP)与脑卒中发生的危险性有着明确的线性关系。1990年Mac Mahen 的多中心前瞻性研究指出,DBP在70~110 mmHg(9.33~14.7 kpa)之间,DBP每增加7.5mmHg,脑卒中的发病率即增加一倍,根据 Framingham的研究,单纯收缩性高血压者SBP>160mmHg时,可使动脉硬化性脑梗塞的发病率显著提高,对>65岁的男性单纯收缩期高血压者比血压脑卒中的流行及发病状态,对高血压患者进行有效的血压控制,及脑卒中后合理的进行血压调整已显示非常重要。
一、 脑卒中后脑细胞对缺血缺氧反应机制
脑细胞对氧异常敏感。由于脑组织的能源储备很少,其主要能源来自葡萄糖的有氧氧化,只有血流中氧和葡萄糖不断供应,是维持精神组织正常和功能必要的条件。血流中断,脑组织缺血、缺氧时将产生一系列变化,造成神经无损伤,这时称为原发性神经元损伤(Primary neuronal damage)。如果及时采 取有效措施,使血流得以再建,氧和葡萄糖的供给及时恢复,则脑组织的缺血性损伤会得到恢复。有时损伤继续加剧,这种现象称为再灌流损伤。若短暂性缺血后血流迅速重建,组织的能量代谢也恢复正常,这时细胞的功能和结构均已正常。但是在数小时或几日后,则会逐渐发生神经元死亡,这种情况称为继发性神经元损伤(secondary neuronal damage )。对上述病理变化了解的越透彻,临床治疗措施越有针对性,则可大地改善血性脑血管病的预后。
1, 原发性神经元损伤。缺血压GBF及代谢均降低,缺血区周围形成一个半暗带(Penum ba),这区带已出现一过性的过度灌流。此时组织损伤可能消退,也可能加剧。在远离病灶的部位,如对侧半球甚至小脑亦出现CBF及代谢的降低,这种现象称为远隔机能障碍。缺血区内血管自身调控机能障碍,血管处于过度扩张状态,此时给予糖类扩血管药物会使病灶区周围正常的脑动脉更加扩张,使血流量增加,会导致病灶区残存的血流流向动脉扩张的区域,形成所谓的脑内盗血现象。后果是缺血区血流不仅不增加,反而减少。事实上,缺血急性期,由于堵塞的动脉再灌通而导致的绝对过度灌流现象。在坏死区域附近由于侧支循环造成相对过度灌流常能见到。
2, 再灌流损伤。由于急性缺血的治疗时间窗(Time window)十分短暂。人们希望能了解再灌流及迟发损伤的机理,以达到临床上可以利用更长一些时间来争取神经元的复原和减少其死亡。
目前认为再灌流损伤机制集中于:①细胞内所增高催发的一系列生理过程;②兴奋性氨基酸的细胞毒作用;③氧自由基过度形成导致神经元损伤;④酸中毒的代谢影响。在少量供O2葡萄糖的情况下,神经元的损伤比缺血更严重,公认的还有氧自由式损伤是导致神经元死亡的最后通路之一。
3, 继发性神经元损伤。短暂脑缺血过后,即局部脑组织代谢已恢复正常。但是数小时或数日后,某些易感部位逐渐出现神经元的死亡,称为继发性或迟发性神经元损伤。此时,谷氨酸NMDA受体兴奋,将诱发乙酰胆碱,去甲肾上腺素、组织胺、5羟色胺及谷氨酸,均能激法磷脂酰肌醇系统,通过磷脂酶降解为甘油二脂(DAC)及三磷酸肌醇(IP3)。IP3作用于内质网膜,使存其内的Ca2+出来进入细胞质,此时缺血时过量放出上述各类递质均会引起Ca2+异常升高。
二、 降压治疗在脑卒中的作用
美国 Framingham的研究发现,血压越高,脑卒中的发病率越高,当有糖尿病,左室肥厚及年龄<50岁的高脂血症患者,脑卒中发生的危险性则越大。据统计约70%~80%脑卒中患者都有高血压及高脂血症史,即使是平日无症状的高血压病人,其发生脑卒中的机会比正常人高出4倍,如果舒张压平均降低5~6mmHg,脑卒中的发生率可下降42%。目前,许循证医学证明,降压治疗对心脑血管器官带来益处。
(1) SHEP的临床试验证实:老年收缩期高血压(SBP>160mmHg但DBP