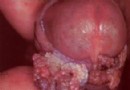
(路透社医学新闻)美国Millennium制药公司于本周一宣布,该公司与Ilex Oncology公司合作研制的抗白血病药物Campath(alemtuzumab)已经获得美国食品和药品管理局(FDA)的批准。
尽管在临床试验中有患者因使用Campath而死亡,但FDA仍批准该药可用于那些烷化剂和氟达拉宾无效的B细胞性慢性淋巴细胞性白血病治疗。
Campath是一种人源性单克隆抗体,主要作用于存在于B和T淋巴细胞上的CD52抗原,从而破坏淋巴细胞。
尽管Campath临床研究中存在30%的死亡率(约半数是治疗相关性死亡,包括血液毒性反应如骨髓增生低下)以及较高的感染率,但是该药总有效率可达到33%,平均有效持续时间为7个月。在2个小规模临床试验中,其有效率分别为21%和29%,平均有效持续时间分别为7和11个月。
在2000年的晚些时候,FDA顾问委员会投票表决,以14票对1票建议加快Campath批准应用,这将允许药物一边在随访研究中搞清未明的问题,一边上市。但是,必须在包装盒上注明应警惕药物的血液毒性、输注反应和治疗相关的感染。
最近该药品已提请欧洲联盟批准以MabCampath的名称在欧盟市场上市,预计在今年下半年可获欧盟的最终批准。
Millennium制药公司称,作为单独用药或联合治疗,Campath正被考虑用于血液肿瘤包括外周和皮肤T细胞淋巴瘤、自体免疫性疾病如多发性硬化的治疗和器官移植排异反应的治疗。